Encarar o diagnóstico e o tratamento de uma doença maligna é uma das mais difíceis experiências pelas quais uma pessoa pode passar. Hoje, no entanto, grande parte das neoplasias pode ser curada, especialmente entre crianças e adultos jovens. Durante a avalanche de informações e decisões que devem ser tomadas no momento do diagnóstico, é muito comum não pensarmos na preservação da fertilidade. Infelizmente, a preservação da fertilidade ainda é muito pouco abordada nas consultas oncológicas, e os pacientes acabam sendo privados dessa ferramenta, que pode ser muito útil após a cura. A questão é delicada, uma vez que, virtualmente, todos os tratamentos oncológicos, como determinados tipo de cirurgia, quimioterapia (QT) ou radioterapia (RT), podem colocar em risco as chances de paternidade futura por conta das sequelas que causam. Isso significa que, mesmo após a cura, é possível que o homem precise lidar com consequências da doença ou do tratamento.
Se considerarmos neoplasias frequentes nos homens jovens, como linfoma ou tumores de testículo, cerca de 50 a 60% dos pacientes apresentarão alterações no espermograma pela simples existência da doença. O tratamento será extremamente resolutivo, mas acrescentará dano ao potencial fértil, pois combate células tumorais que se dividem rapidamente. O grande problema reside no fato de que os tratamentos não atuam apenas nas células neoplásicas, mas em todas as células que se multiplicam rapidamente. O tecido reprodutivo no interior dos testículos apresenta exatamente essa característica, sendo, portanto, muito susceptível à ação desses tratamentos. A primeira grande mensagem, consequentemente, é que todos os tratamentos oncológicos podem trazer risco de esterilidade no futuro, e todos os homens que receberem tratamentos merecem medidas que preservem seu potencial fértil.
DETERMINAÇÃO DO RISCO À FERTILIDADE
Para determinarmos se o risco será menor ou maior, precisamos saber exatamente qual será a modalidade (quimio ou radioterapia) e quais medicamentos serão utilizados.
- Risco alto: azoospermia definitiva ou prolongada: QT que envolvem drogas chamadas alquilantes (ex.: ciclofosfamida, busulfan, procarbazina), utilizadas em sarcomas, leucemias, linfomas, neuroblastoma, por meio de tratamentos como o BEACOPP e MOPP; RT em pelve (para tumor testicular), crânio ou corpo inteiro (previamente a transplante de medula). De modo geral, a radioterapia tem grande potencial esterilizante, principalmente em doses altas (>2,5Gy – radiação equivalente a 250 radiografias de tórax).
- Risco intermediário: chances reduzidas de azoospermia definitiva: QT contendo cisplatina ou carboplatina, QT para tumor testicular (BEP).
- Risco baixo: alterações seminais temporárias, na maioria das vezes: QT clássica sem drogas alquilantes para linfomas e leucemias, como ABVD, CHOP, COP; RT de baixas doses para tumor testicular (<0,7Gy – radiação equivalente a 70 radiografias de tórax).
- Risco muito baixo: praticamente, não há impacto na produção espermática: radioiodoterapia, utilizada para tumores de tireoide.
- Risco indeterminado: modalidades ainda recentes: anticorpos monoclonais (abciximab, cetuximab) e inibidores da tirosina-quinase (erlotinib, imatinib).
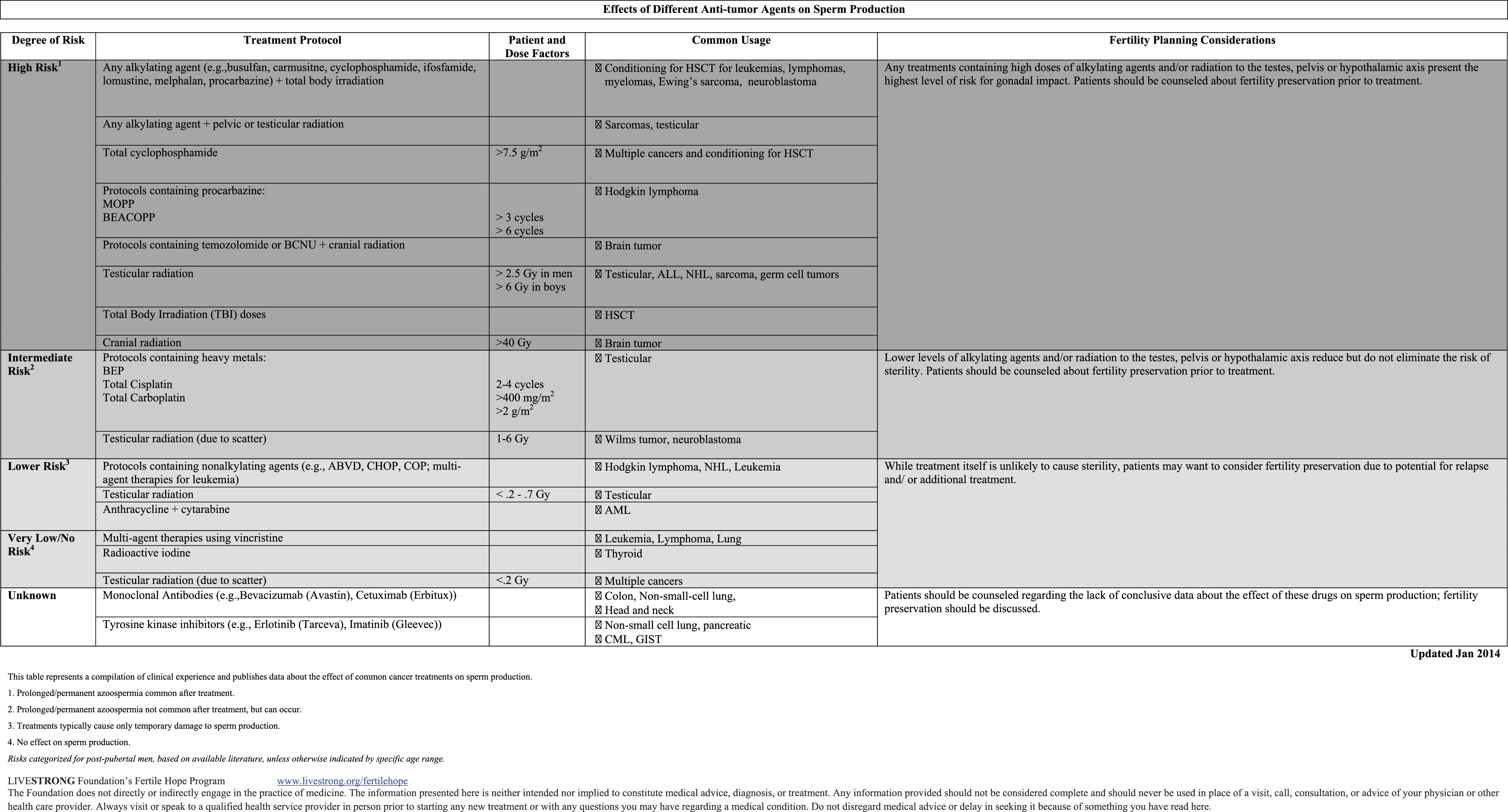
Fonte: Loren AW, et al. Fertility Preservation for Patients With Cancer: American Society of Clinical Oncology Clinical Practice Guideline Update. J Clin Oncol 31:2500-2510. Data supplement disponível em: http://www.instituteforquality.org/sites/instituteforquality.org/files/fp_data_supplements_012914.pdf
Algumas cirurgias oncológicas, também, podem trazer problemas à fertilidade:
- Remoção da próstata para tratamento de tumores (prostatectomia radical): não há impacto na produção de espermatozoides, mas elimina-se definitivamente a possibilidade de gravidez natural por remoção de porções do trajeto espermático. Cria-se uma situação de azoospermia obstrutiva.
- Linfadenectomia retroperitoneal: remoção dos gânglios abdominais durante cirurgias de remoção de tumores renais ou testiculares: ocorre dano a pequenos ramos nervosos que comandam a ejaculação: mantém-se a produção espermática, mas pode ocorrer uma situação chamada ejaculação retrógrada, em que os espermatozoides saem na ejaculação e acumulam-se na bexiga, junto com a urina.
- Orquiectomia radical: remoção testicular por tumores: há remoção do órgão que produz os espermatozoides. Isso é particularmente crítico quando se planeja a remoção de testículo único.
- Ressecção transuretral de próstata ou bexiga (RTU): há dano do mecanismo muscular de ejaculação, o que leva à ejaculação retrógrada.
Muitos homens que foram submetidos à QT ou RT no passado e planejam ter seus filhos após a cura se preocupam com os riscos que os tratamentos podem trazer à saúde das crianças. Sabemos que esses tratamentos podem propiciar algum risco de teratogenicidade durante seu uso e nos primeiros anos após o término. Depois de certo tempo, os riscos de saúde nos filhos não parecem ser maiores do que os riscos de qualquer pessoa. Dessa forma, recomendamos alguns cuidados:
- Durante o tratamento, sugere-se evitar gravidez com métodos contraceptivos, pelo alto risco de teratogenicidade.
- Após o término do tratamento, mesmo que não tenha ocorrido azoospermia, sugere-se manter a contracepção por 1 ano (se o espermograma não tiver zerado em nenhum momento) ou 2 anos (se em algum momento houve azoospermia). Após esse período, o paciente pode buscar a gravidez. Evidentemente, se houve criopreservação (congelamento) de espermatozoides antes do início do tratamento, eles podem ser utilizados para terapia de reprodução assistida (TRA) em qualquer momento.
- Recomenda-se a criopreservação seminal ANTES do início de qualquer tratamento oncológico. Após o início de QT ou RT, já pode haver dano e risco de teratogenicidade, mesmo existindo espermatozoides nos primeiros meses, não se recomenda o congelamento.
COMO PRESERVAR A FERTILIDADE DO HOMEM?
Preservação de espermatozoides – criopreservação ou congelamento
O congelamento (ou criopreservação) de espermatozoides é o método clássico para se preservar a fertilidade antes do início da QT ou RT. Virtualmente, todos os pacientes que serão submetidos a tratamento oncológico devem receber a oportunidade de congelar seu sêmen. Qualquer quantidade de espermatozoides móveis ou viáveis pode ser congelada, de forma que não é necessário que o espermograma seja normal para a preservação. A quantidade de amostras a ser congelada deverá ser discutida caso a caso, levando-se em consideração o planejamento familiar e a qualidade do material ejaculado. Amostras com muitos espermatozoides poderão ser divididas em diversos contêineres para congelamento, ao passo que amostras prejudicadas renderão menos alíquotas. Em linhas gerais, quando há possibilidade de ejaculação e existem espermatozoides no líquido, pode-se realizar o congelamento. O processo de congelamento e descongelamento é extremamente seguro, sem riscos documentados à saúde dos futuros filhos. Todavia prevemos que cerca de metade dos espermatozoides pode não tolerar o trauma do descongelamento, o que justifica procurarmos congelar uma quantidade mínima que garanta o sucesso do descongelamento. Adicionalmente, faz-se um teste de descongelamento, de uma pequena amostra congelada separadamente, para definirmos como será o comportamento dos espermatozoides quando as alíquotas de preservação forem descongeladas. Além disso, conseguimos informações adicionais a respeito do número total de coletas a serem sugeridas ao paciente.
PROTEÇÃO TESTICULAR DURANTE A RADIOTERAPIA
Quando se planeja RT testicular ou na região pélvica, é importante utilizarmos dispositivos de proteção ao outro testículo, uma vez que a radiação pode danificar tecidos saudáveis nas proximidades. Proteger o testículo que não será tratado (testicular shielding) é uma estratégia simples e minimiza grandemente o risco de esterilidade.
Coletas assistidas – coleta na urina, vibroestimulação (VE), eletroejaculação (EEJ)
Em determinadas circunstâncias, a ejaculação pode não ser possível por conta de trauma raquimedular ou cirurgias prévias que causem ejaculação retrógrada. No caso dos pacientes cadeirantes, podemos adotar técnicas habitualmente utilizadas para obtenção de espermatozoides, como a VE ou a EEJ. Homens submetidos a cirurgias urológicas ou pélvicas e que sejam portadores de anejaculação (situação em que há orgasmo “seco”, sem saída de líquido seminal) podem experimentar a ejaculação retrógrada, sendo necessário capturar os espermatozoides na urina ou até mesmo no interior da bexiga. Essas técnicas podem ser usadas a fim de se obter espermatozoides para congelamento antes do início de QT ou RT, ou, até mesmo, como estratégia pós-tratamento, como ferramenta de manejo de sequelas de tratamento quando já tiver transcorrido o período de 1-2 anos de recuperação seminal.
CAPTURA CIRÚRGICA DE ESPERMATOZOIDES
- Antes do tratamento: em homens portadores de azoospermia, não conseguiremos congelar espermatozoides obtidos por masturbação. Esses casos precisam ser conduzidos da mesma forma que os casos habituais de azoospermia, assim, aplicando-se as técnicas de captura cirúrgica usuais, como a microdissecção testicular (microTESE) ou a aspiração microcirúrgica de epidídimo (MESA). Em casos muito selecionados, podemos realizar a microTESE durante o tratamento cirúrgico de testículo único, procurando espermatozoides no testículo removido, em um procedimento muito peculiar conhecido como onco-TESE.
- Após o tratamento: após tratamentos que tornem o paciente azoospérmico, ainda existe possibilidade de obtermos espermatozoides. Da mesma forma que qualquer indivíduo portador de azoospermia não obstrutiva, pois podem existir mínimas quantidades de produção espermática que tenham suportado o trauma medicamentoso ou radioterápico. Essas pequenas ilhas, quando presentes, produzirão quantidades de espermatozoides que não serão suficientes para chegar à ejaculação. Se respeitarmos o período de 1-2 anos de recuperação testicular, espermatozoides poderão ser encontrados em até 55% dos homens, sem que haja o aumento de risco de problemas de saúde à prole.
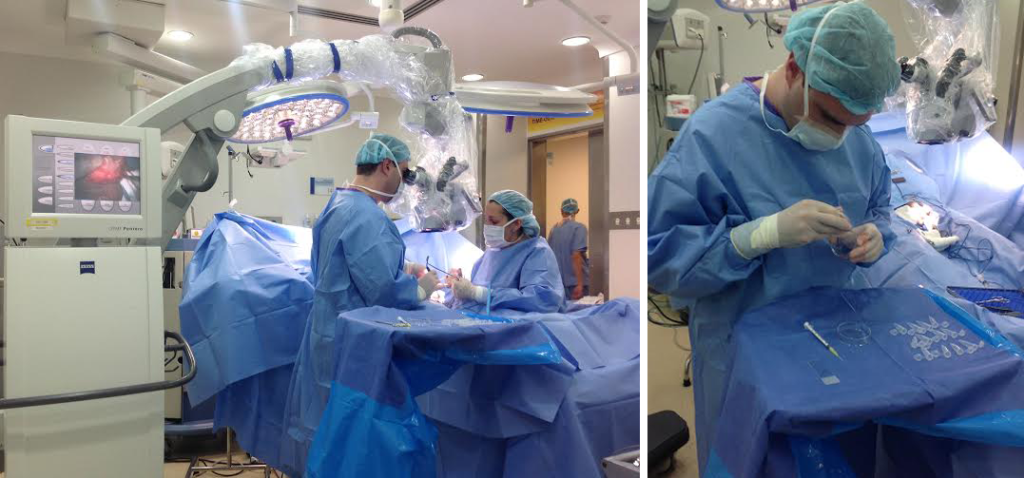
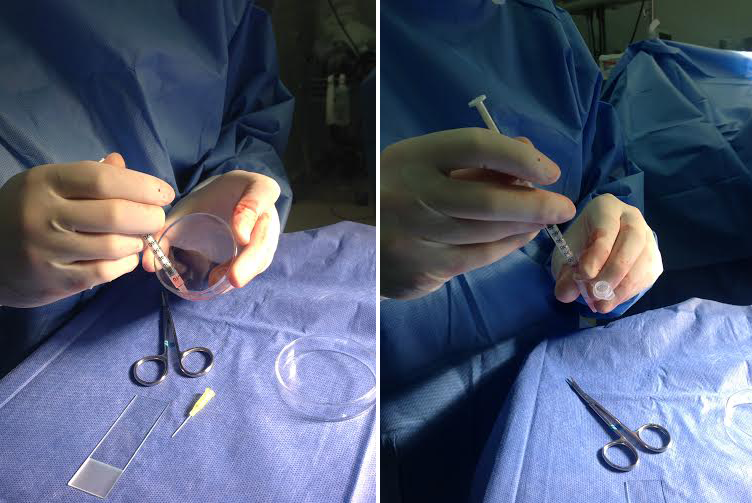
Fonte: arquivo pessoal
FUTURO: MODALIDADES AINDA EXPERIMENTAIS
Algumas modalidades podem ser oferecidas, mas ainda em caráter experimental, uma vez que as características de uso futuro ainda não foram estabelecidas.
Em meninos pré-púberes que ainda não ejaculam, pode-se realizar a retirada cirúrgica de material testicular para congelamento. No entanto, por serem muito jovens, os meninos ainda não contam com espermatozoides maduros no interior dos testículos. Dessa forma, é necessário que se congele células ainda imaturas (células-tronco testiculares, ou espermatogônias) para uso em futuras técnicas (que podem envolver amadurecimento celular com finalidade de formação de espermatozoides utilizáveis ou confecção de fragmentos a serem enxertados novamente no homem, após sua cura).
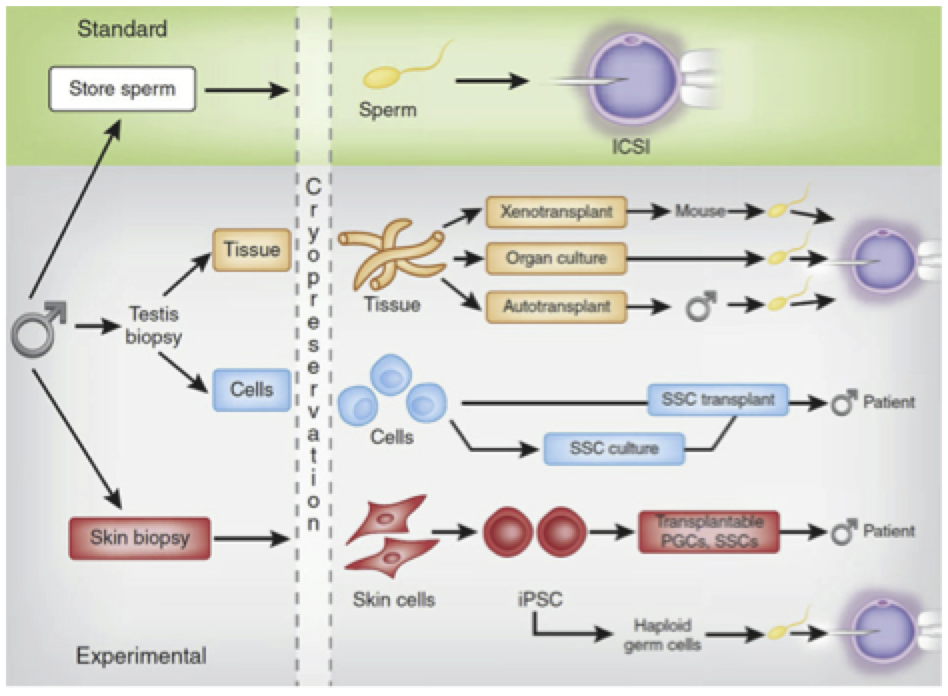
Fonte: Clark AT, et al. Fruitful progress to fertility: male fertility in the test tube. Nature Medicine 17,1564–1565 (2011). Disponíivel em: http://www.nature.com/nm/journal/v17/n12/fig_tab/nm.2594_F1.html
A forma de congelar essas células ainda não foi completamente definida e, portanto, casos assim precisam ser criopreservados de maneira diferente de um espermatozoide maduro. Como essas técnicas são embrionárias e não podem ser oferecidas de uma maneira consistente, essa modalidade deve ser encarada como uma ferramenta factível, porém com uso futuro ainda indeterminado.
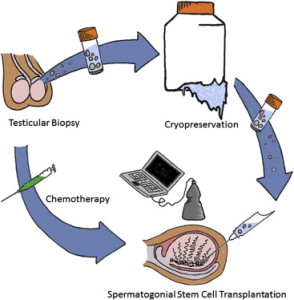
Fonte: Hermann BP, et al. Spermatogonial stem cell transplantation into rhesus testes regenerates spermatogenesis producing functional sperm.
Cell Stem Cell. 2012 Nov 2;11(5):715-26
Dr. Guilherme Leme de Souza

